Kohlenstoff-Brennstoffzellen
|
Im Jahr 1897 erhielt der USAmerikaner W. Jacques ein Patent
auf eine Brennstoffzelle, deren Anode aus Kohlenstoff und
Anode aus Sauerstoff bestanden, die über den Elektrolyten
KOH leitend verbunden waren: Die Geburtsstunde der
Kohlenstoff-Brennstoffzelle.
In den folgenden Jahren geschah nichts mit dieser Erfindung,
denn andere Wissenschaftler (wie z.B. F. Haber) konnten die
Energiewandlung mithilfe dieser Brennstoffzelle nicht
bestätigen. Dies gelang erst 1973 in Stanford/USA. Seitdem
sind wesentliche Fortschritte in der Entwicklung einer
derartigen Brennstoffzelle erzielt worden.
|
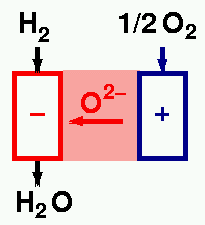
Der prinzipielle Aufbau einer
Kohlenstoff-Brennstoffzelle ist sehr ähnlich dem einer
Wasserstoff-Brennstoffzelle, wie in den Abbildungen unten
gezeigt, die aus den entsprechenden Abbildungen in  Energie2
abgeleitet wurden. Energie2
abgeleitet wurden.
2
H2 + O2 -> 2 H2O
|
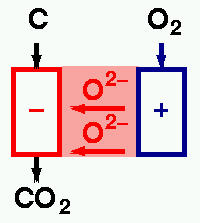
C
+ O2 -> CO2
|
Die fundamentalen Reaktionen, mit deren Hilfe die chemische
Energie direkt in elektrische Energie gewandelt wird,
lauten:
An der Anode
H2 + O2-
-> H2O + 2 e-
|
C
+ 2 O2- -> CO2 + 4 e-
|
An der Kathode
1/2 O2 + 2 e-
-> O2-
|
O2
+ 4 e- -> 2 O2-
|
Die Potenzialdifferenzen (elektrische Spannungen) U zwischen Kathode und
Anode wurden in  Energie2
berechnet, sie betragen Energie2
berechnet, sie betragen
theoretisch
1.2 V
|
praktisch
1.0 V
|
|
theoretisch
1.0 V
|
praktisch
0.8 V
|
|
Die Kohlenstoff-Brennstoffzelle besitzt aber gegenüber der
Wasserstoff-Brennstoffzelle zwei entscheidende Vorteile:
- Der Ladungszustand von Kohlenstoff ist doppelt so groß
wie der eines Wasserstoffmoleküls. Daher ist auch im
ersten Fall die (Ladungs-)Stromdichte doppelt so hoch,
wenn die Anzahldichten an der Anode gleich groß sind.
- Die Gasvolumina vor und nach der Reaktion sind im Fall
der Kohlenstoff-Brennstoffzelle gleich groß, dagegen
verschieden im Fall der Wasserstoff-Brennstoffzelle. Das
bedeutet, dass sich die Entropie im ersten Fall fast
nicht verändert, der gesamte Heizwert H kann daher
vollständig in elektrische Energie Wel
gewandelt werden.
Daher ist der Nutzungsgrad der Kohlenstoff-Brennstoffzelle
mit 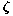 = 0.8 sehr groß, verglichen mit = 0.8 sehr groß, verglichen mit 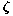 = 0.5 im Fall der Wasserstoff-Brennstoffzelle.
= 0.5 im Fall der Wasserstoff-Brennstoffzelle.
|
Das besondere Problem besteht
darin, die erforderlichen Teilchendichten für den
Kohlenstoff zu erreichen. Eine Möglichkeit bietet die
Hydropyrolyse, bzw. Pyrolyse, mit deren Hilfe Kohle bzw.
Kohlenwasserstoffe in Nanoteilchen aus Kohlenstoff (Ruß)
zerlegt werden können. Darüber hinaus können aber z.B. auch
Abfallstoffe aus der Petrochemie oder sogar Biomasse mit
geeigneten Verfahren zerlegt und in einer
Kohlenstoff-Brennstoffzelle eingesetzt werden. Für die
Biomasse ist dies wahrscheinlich die Technologie mit den
höchsten Nutzungsgraden (siehe auch  Kap. 3.2). Kap. 3.2).
|
Unter optimalen Bedingungen
beträgt die Leistungsflächendichte einer derartigen Zelle
etwa
I = 8 · 10 3 kWh a -1 m -2.
Das sollte verglichen
werden mit der mittleren Sonnenintensität in
Deutschland, die nur einen Wert von
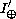 = 1 · 10 3
kWh a -1 m -2
erreicht, also 8mal geringer ist.
|
In der Entwicklung zu einem
praktisch nutzbaren Prototyp durch das  Lawrence
Livermore National Laboratory wird als Elektrolyt eine
Karbonatschmelze (z.B. Na2CO3)
verwendet, die von 2 Nickelelektroden begrenzt ist.
Kathodenseitig befindet sich ein Brei aus
Kohlenstoff-Nanoteilchen und geschmolzenem Karbonat,
anodenseitig strömt Luft (O2) an der Elektrode
vorbei. Die Reaktionsgleichungen lauten in dieser
Ausführung: Lawrence
Livermore National Laboratory wird als Elektrolyt eine
Karbonatschmelze (z.B. Na2CO3)
verwendet, die von 2 Nickelelektroden begrenzt ist.
Kathodenseitig befindet sich ein Brei aus
Kohlenstoff-Nanoteilchen und geschmolzenem Karbonat,
anodenseitig strömt Luft (O2) an der Elektrode
vorbei. Die Reaktionsgleichungen lauten in dieser
Ausführung:
An der Anode: C + 2 CO32-
-> 3 CO2 + 4 e-
|
An
der Kathode: O2 + 2 CO2 + 4
e- -> 2 CO32-
|
Daraus wird ersichtlich, dass der Elektrolyt selbst
verbraucht wird, d.h. er muss durch CO2-Zugabe
immer wieder erneuert werden1). Außerdem gibt es
ein weiteres Problem: Das Karbonat schmilzt erst bei ca.
1100 K, die Brennstoffzelle muss also hoch erhitzt werden.
Das erfordert zusätzlich thermische Energie, die sich aber
u.U. mithilfe von  Konzentratoren aus
der Sonnenstrahlung wandeln lässt. Wegen der notwendigen und
kontinuierlichen Ausrichtung der Konzentratorelemente ist
das sicherlich eine Technik, die sich nur mit stationären
Wandlungsanlagen in einem Gebiet verwirklichen lässt, in dem
die Sonnenstrahlung nur aus der direkten Komponente besteht.
In Deutschland sind derartige Gebiete nicht vorhanden. Konzentratoren aus
der Sonnenstrahlung wandeln lässt. Wegen der notwendigen und
kontinuierlichen Ausrichtung der Konzentratorelemente ist
das sicherlich eine Technik, die sich nur mit stationären
Wandlungsanlagen in einem Gebiet verwirklichen lässt, in dem
die Sonnenstrahlung nur aus der direkten Komponente besteht.
In Deutschland sind derartige Gebiete nicht vorhanden.
|
1) Es ist
merkwürdig, dass dieses Problem in keinem der vorliegenden
Berichte erwähnt wird. Dabei ist es offensichtlich, wenn man
die Reaktionsgleichungen betrachtet.
|


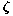 = 0.8 sehr groß, verglichen mit
= 0.8 sehr groß, verglichen mit 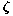 = 0.5 im Fall der Wasserstoff-Brennstoffzelle.
= 0.5 im Fall der Wasserstoff-Brennstoffzelle. 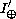 = 1 · 103
kWh a-1 m-2
erreicht, also 8mal geringer ist.
= 1 · 103
kWh a-1 m-2
erreicht, also 8mal geringer ist.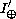 = 1 · 103
kWh a-1 m-2
= 1 · 103
kWh a-1 m-2